재발성 단순 요로감염
급성 요로감염 이후의 재발성 감염은 성인 여성에게서 흔히 발생한다. 잦은 빈도의 재발성 요로감염을 동반하는 여성에 대한 치료는 환자나 의사 모두에게 번거로운 과정이다. 환자는 요로감염이 재발할 때마다 하부요로증상, 권태, 일상생활의 제한을 경험하고, 의사는 병태생리에 대해 알려진 바가 적은 질환에 대해 환자를 상담하는 것에 어려움을 겪게 된다. 재발성 요로감염에 대한 예방법은 현재로서는 제한적인 상황으로, 대부분의 경우 효율이 떨어지고 예상치 못한 부작용을 동반하기도 한다. 본지침에서는 건강한 성인 여성에서 재발성 요로감염의 치료에 대해 가능하고 효율적인 권고안을 정립하고자 한다.
재발성 요로감염의 개요와 원인
요로감염 후 재발은 건강한 성인 여성에서 흔히 발생한다.1 (LE: 2) 한 연구에서 건강한 여대생들을 대상으로 요로감염 후 6 개월 간 추적 관찰한 결과 20.9% 에서 적어도 1 회의 증상을 동반한 재발이 발생했다고 보고하였다.2 또 다른 연구에서는 179 명의 핀란드 여성들을 대장균에 의한 요로감염 후 1 년 간 추적 관찰한 결과 44%에서 적어도 1 회 이상, 5% 에서 3 회 이상의 재발이 발생했다고 보고하였다.3 질병의 자연사 연구에 따르면 요로감염은 최초 발생 이후, 3-4 개월 간 집중적으로 발생한다고 한다. 재발 가능성이 제일 높은 시기는 30 일에서 60 일 후로서, 이후 재발성 요로감염의 빈도는 감소한다.4,5
재발성 요로감염 원인의 대부분은 생식기나 항문직장부위와 같은 요로계 외적인 요인에서 기인하는 재감염으로 알려져 왔다. 그러나 최근에는 요로병원성의 E. coli (UPEC:uropathogenicE. coli) 가 요로상피에 침입하여 잠재적으로 세포 내부에 세균을 비축(QIRS:quiescent intracellular bacterial reservoirs) 하는 것으로 확인되었고 QIRS 가 지속적인 세균의 생존과 재발성 요로감염의 요인을 제공한다고 추정된다.6-8
진단과 평가
재발성 요로감염의 치료에 있어서 첫 단계는 자세한 병력청취와 세밀한 이학적검사이다. 올바른 병력 청취를 통해 과거 요로감염의 횟수, 빈도를 알 수 있고 부가적으로 폐경 여부, 최근 항생제 복용, 성관계 이력(상대방이 몇 명인지, 새로운 상대가 있는지, 살정제의 사용 여부, 차단식 피임 수단의 사용 여부)을 알 수 있다. 이학적 검사는 질내 상태와 골반 장기 탈출 여부를 살필 수 있어야 한다. 요도게실 및 Skene gland 의 낭종이나 감염 여부를 알 수 있어야 한다. 소변 배양검사는 일반적으로 권고되나 (LE: 4,GR: A) 단순 하부요로 감염의 경우 추가적인 영상학적 검사는 필요하지 않은 경우가 대부분이다.1 (LE: 1, GR: B) 100 명의 건강한 여성을 대상으로 한 연구에서 이들의 복부 단순 촬영, 방광내시경, 경정맥신우조영술 및 복부 초음파는 대부분 정상 소견을 보였다고 한다.9 만약 과거력이나 이학적 검사에서 복합성 요로감염을 시사하는 소견이 있을 경우 배뇨 후 잔뇨 검사, 요로계 초음파 및 방광 내시경과 같은 검사의 추가 여부를 결정하는 것이 좋다. (LE: 4, GR: B) (Table 1)
Table 1. 재발성 요로감염 시 추가 검사가 필요한 경우
| • 과거 비뇨기과적 수술 이나 손상 병력이 있는 경우
• 요로감염이 해결된 후에도 육안적 혈뇨가 지속되는 경우 • 과거 요로결석 병력이 있는 경우 • 낮은 요속 및 많은 잔뇨와 같이 방광출구 폐색이 의심되는 경우 • 요배양검사에서 urea-splitting 세균 동정된 경우 (예, Proteus, Yersinia) • 감수성있는 항생제 치료에도 불구하고 세균이 지속적으로 동정되는 경우 • 과거 복부 또는 골반의 암성 종양 병력이 있는 경우 • 심한 당뇨 또는 면역억제 질환이 있는 경우 • 공기뇨, 분변뇨, 혐기성 세균뇨, 또는 게실염 병력이 있는 경우 • 반복적인 신우신염 (발열, 오한, 구토, 측복통)이 있는 경우 • 요로감염이 호전 되었음에도 불구하고 무증상 혈뇨가 지속되는 경우 |
치료
행동 교정 (Behavioral modifications)
한 연구에서 재발성 요로감염이 발생하는 여성의 경우 성적 활동력이 다양하다고 보고하였다. 성적 활동이 활발할수록, 최근 12 개월 간의 성적 활동이 활발할수록, 최근 1 개월 간의 성관계 빈도가 높을 수록 재발성 요로감염의 위험성 증가와 독립적인 연관성이 있다고 하였다.5,10 또한 살정제의 사용, 차단식 피임기구 사용, 새로은 성관계 상대, 다수의 성관계 상대 여부 또는 성매개 질환의 과거력 역시 재발성 요로감염의 빈도를 증가시키는 독립적인 위험요인으로 알려져 있다.10 성적으로 활발한 여성의 경우 차단식 피임기구나 살정제를 사용하고 있을 경우 중단하는 것이 권장되나 (LE: 3, GR: B) 일반적으로 알려져 있는 위험 요인 즉, 성관계 전후 배뇨 유무, 배뇨 횟수, 수분 섭취량, 개인 위생 증진(항문을 닦는 방향), 온좌욕, 질세척, 탐폰 사용의 경우 재발성 요로감염의 발생과 뚜렷한 연관을 보이지 않았다는 연구 결과가 있다.10,11 즉 수분 섭취량 증가, 개인위생의 변화 및 성관계 전후의 배뇨가 재발성 요로감염의 예방을 위해 반드시 필요하다고 할 정도의 근거는 성립되지 않았다. 비만과 요로감염과의 연관성을 연구한 보고가 있는데 비만인 여성이 정상 체중의 여성보다 요로감염을 진단받을 확률이 높은 것으로 보고하였다. 그러나 BMI 30 에서 34.9 인 경우에만 통계적으로 유의했다고 한다. (OR 1.22, CI 1.15~1.28)12 따라서 향후 체중 감소와 관련된 연구를 통해 비만을 요로감염 발생의 위험인자로 볼 수 있는지의 여부에 대해서는 추가적인 확인이 필요하다.
Estrogen 보충
질 위축을 동반한 폐경기 여성에서 estrogen 보충이 재발성 요로감염의 발생을 감소시킬 수 있는지에 대한 다수의 연구가 진행되었다.13 9 개의 RCT 에서 3,345 명의 폐경 여성을 대상으로 연구를 진행하였고 경구용 estrogen 은 재발성 요로감염의 발생을 억제하지 못했고 질 출혈과 유방 통증과 같은 부작용을 일으킨다는 결론을 보고하였다.13 2 개의 RCT 에서는 estrogen 이 국소적으로 질에 투여될 경우 재발성 요로감염의 빈도를 줄인다고 보고하였다.14 Raz 와 Stamm15 은 8 개월 간의 연구에서 erteogen 의 질 도포가 재발성 요로감염을 유의하게 감소(1 년당 0.5 vs 5.9 회/명, P < 0.001)시킨다고 보고하였다.15 폐경 후 여성에서 estrogen 을 씌운 vaginal ring 을 사용한 결과 36 주 후 요로감염의 발생과 관련한 risk ratio 가 0.64(95% CI. 0.47~0.86)로 감소한다고 보고한 연구도 있다.16 질 위축을 보이는 폐경기 여성의 질내 estrogen 의 도포는 재발성 요로감염의 예방에 효과적이고 안전하다고 여겨진다. (LE: 2, GR: B)
항생제를 이용한 예방법
항생제 예방 요법이 시행되기 전에, 기존의 요로감염은 치료 1~2 주 후 추적 요배양검사를 통해 치료가 완전히 종결되었음이 확인되어야 한다. (LE: 4, GR: A) 재발성 요로감염에 대한 항생제 예방 요법은 반드시 충분한 상담과 행동교정 요법이 이루어진 후, 해당 방법이 성공적이지 않았을 경우에 한해 시행되어야 한다.17 (LE: 4, GR: B) 임상적으로 유의한 잔뇨량은 반드시 치료가 선행되어야 하며 폐경기 여성에서는 호르몬 보충요법 또한 고려되어야 한다. 반복적인 단순 요로감염의 경우 항생제 자가 치료법(Self-start therapy)이 고려될 수 있다.18 (LE: 2, GR: A).
항생제 자가 치료법 (Self-start therapy)
항생제 자가 치료법(self-start therapy)은 환자들에게 증상이 발생할 경우 진단 및 치료를 할 수 있는 지침과 약제를 제공하는 것이다. 재발성 요로감염 환자 중 동기가 충분하고 자가진단 및 치료방법을 숙지하고 있는 경우에는 자가진단의 정확도가 높을뿐더러(88%-92%) 효과적인 치료 역시 가능하다.18-20 이 방법은 지속적인 예방적 항생제 투여에 비해 높은 재감염률(연간 2.2 회 vs 연간 0.2 회)을 보이지만,19 만족도는 더 높고 임상적 및 미생물학적인 치료 경과도 빠르며 부작용은 더 낮다.18-20 이러한 방식으로 단순 급성 방광염과 같은 재발성 요로감염을 효과적으로 치료할 수 있다. (LE: 2, GR: B) 사전에 환자 개개인에 대한 알러지, 특징적인 항생제 저항성에 대한 심사숙고가 선행되어야 한다. 미국과 유럽의 감염병 학회는 nitrofuratoin macrocrystals 100mg, BID 로 5 일 또는 trimethoprim/sulfamethoxazole 160/800mg, BID 로 3 일 또는 fosfomycin trometamol, 3g, QD 로 1 일 또는 pivmecillinam, 400mg, BID 로 5 일 투여를 권장한다. 만약 이와 같은 항생제를 복용할 수 없을 경우 fluorquinolone 또는 beta lactam 을 투여할 수 있다.21
성관계 후 예방적 항생제 복용 (Postcoital prophylaxis)
성적으로 활동적인 여성일 경우 성관계 후 1 회의 항생제 복용이 재발성 요로감염의 예방에 효과적일 수 있다. (LE: 2, GR: B) RCT 에서 재발성 요로감염의 과거력이 있는 건강한 폐경 전의 여성을 대상으로 성관계 후 1 회의 항생제(trimethoprim/sulfamethoxazole) 와 placebo 복용을 비교하였고 placebo 를 복용한 11 명 중 9 명에서 UTI 가 발생하였고 (3.6 UTI/patient-year) 항생제를 복용한 16 명 중 2 명에서 UTI 가 발생하였다. (0.3 UTI/patient-year) Trimethoprim/sulfamethoxazole 의 경우 성관계의 빈도와 관계 없이 효과적이었다고 한다.22 성관계 후의 예방적 복용은 지속적은 예방 약제 투여와 유사한 효과일 것이라고 생각된다. 재발성 요로감염의 과거력이 있는 152명의 여성을 무작위로 나눠서 매일 또는 성관계 후 ciprofloxacin 125mg 을 투여한 연구에서 두 군간의 발생률은 모두 감소하였고(3.66 -> 0.031 episode per year vs 3.62 ->0.043 episode per year) 통계학적으로 유의한 차이는 없었다. (P = 0.7)23 Table 2 은 성관계 후 예방적 항생제 복용에 사용될 수 있는 약제들이다.
Table 2. 재발성 요로감염 예방을 위한 성관계 후 예방적 항생제 복용
| 항생제 종류 | 용량 (단회 용법) |
|---|---|
| Trimethoprim-sulfamethoxazole | 80 mg/400 mg |
| Nitrofurantoin macrocrystal* | 50 mg or 100 mg |
| Cefaclor | 250 mg |
| Ciprofloxacin | 250 mg |
| Norfloxacin | 200 mg |
| Ofloxacin | 100 mg |
*2016 년 4 월 현재, 국내 사용불가
예방적 항생제의 지속적인 복용 (Continuous prophylaxis)
1,120 명의 건강한 여성을 대상으로 한 19 개 RCT 에 대해 Cochrane review 결과에서는 지속적인 예방적 항생제 투여는 위약과 비교하였을 때 투여 기간 동안 UTI 의 재발을 감소시키는 것으로 알려졌다. (LE 2, GR 2) 특히 예방적 항생제 투여의 중단에도 재발성 요로감염의 빈도는 양 군에서 차이가 없었다(RR 0.82; 95% CI, 0.44-1.53). 부작용의 경우 예방적 항생제를 투여하는 군에서 높았고(RR 1.58, 95% CI, 0.47-5.28) 13.5 회의 투여마다 부작용이 발생하였다. 연구 간 설계 및 진행에 있어 차이가 있었기에 각각의 항생제에 대한 효율성이나 안전성에 대한 비교는 불가능하였다.17 지속적인 예방적 항생제의 투여를 위한 이상적인 용량이나 일정은 아직 불명확하며, 매일 복용과 이틀에 한 번 복용하는 경우의 비교는 없으나, 일주일 단위의 투여는 매달 단위의 투여보다는 더 효과가 있다는 것이 알려졌다. Guibert 등의 연구에서는 일주일 단위와 매달 단위로 400mg 의 pefloxacin 을 여성 재발성 요로감염 환자에게 투여하였고 4년 간의 관찰에서 일주일 단위의 경우 185 명 중 17 명(9.1%) 에서 적어도 1 회 이상의 재발이 발생하였고 매달 단위의 경우 176 명 중 52 명(29.5%) 에서 재발이 발생하였다고 보고하였다. (P < 0.0001)24
Table 3 에 지속적인 예방적 투여에 흔히 사용되는 항생제를 정리하였다. 6 개월 이상 nitrofurantoin 을 복용해야 하는 경우 6 개월마다 간기능 검사 및 흉부촬영이 필요하다.25
Table 3. 재발성 요로감염 예방을 위한 예방적 항생제 지속 요법
| 항생제 종류 | 용량 | 빈도 |
|---|---|---|
| Trimethoprim-sulfamethoxazole | 40 mg/200 mg | Daily or 3x/ week |
| Nitrofurantoin macrocrystal* | 50-100 mg | Daily |
| Cefaclor | 250 mg | Daily |
| Fosfomycin | 3g every 10 d | 3g every 10 d |
*2016 년 4 월 현재, 국내 사용불가
항생제 외의 예방법
크랜베리
프로안토시아니딘은 크랜베리에서 높은 함량을 가진 성분으로, 여러 실험 연구에서 프로안토시아니딘 용량 의존적으로 요로상피세포에 대한 대장균의 부착과 탈착이 일어난다고 하였다.26-28 몇몇 임상실험 결과 크랜베리(Vacciniummacrocarpon)는 여성의 하부요로감염 발생률을 감소시키는 효과가 있는 것으로 알려졌다.29,30 (LE: 1, GR: C). Stothers30 는 150 명의 재발성 요로감염에 이환된 건강한 여성(21 세에서 72 세)을 대상으로 위약, 위약 주스, 크랜베리 정 또는 크랜베리 주스와 위약을 무작위적으로 투여하였다. 12 개월 간의 관찰 동안 크랜베리 정과 크랜베리 주스를 복용한 군에서 위약군과 비교할 때 적어도 1 회의 증상을 동반한 요로감염의 재발을 경험한 환자의 비율이 의미있게 낮았다고 한다. (20%; 크랜베리 주스, 18%; 크랜베리 추출물 vs 32%; 위약; P < 0.05)
그러나 대규모의 임상 실험에서는 이견이 있다. 최근의 이중맹검 RCT 는 크랜베리 주스가 재발성 요로감염의 이환을 예방하지 못했다고 발표했다; 319 명의 대학 여성들이 8 온스의 27% 저지방 크랜베리 주스 또는 위약 주스를 하루 2 회 섭취하였다. 6 개월간 또는 재발성 요로감염이 발현되기까지 추적 관찰하였고 재발률은 두 군에서 유사하였다고 한다. (19.3% vs 14.6%, P = 0.21)31 크랜베리는 재발성 요로감염의 예방에 있어서 유용할 것으로 생각되나 표준화를 위한 연구가 선행될 필요가 있다.
아스코르빈산
아스코르빈산(vitamin C)의 경우 소변의 산성화를 통해 재발성 요로감염의 예방에 도움이 되기에 권장되곤 한다. 그러나 건강한 성인 여성을 대상으로 이러한 현상을 뒷받침 해줄 만한 근거는 부족하다. Foxman 과 Chi 는 젊은 여성을 대상으로 음식을 통한 vitamin C 의 섭취와 요로감염의 위험성 감소는 거의 연관이 없다고 발표했다.11 110 명의 임산부들을 대상으로 한 다른 연구에서는 ferrous sulfate 200mg/day, folic acid 5mg/day 및 ascorbic acid 100mg/day 를 복용한 군과 ferrous sulfate 와 folic acid 만을 복용한 군으로 나누어 비교하였고 3 개월 간 ascorbic acid 를 투여받은 군에서 요로감염의 빈도가 낮았다고 보고했다.32 현재 체외 실험의 결과에서 비타민 C 는 소변에서 정균 효과가 있다고 하며, 이는 소변의 pH 를 감소시키는 것 보다는 소변 내 nitrites 를 활동성의 nitrogen oxides 로 환원시킴으로써 효과가 발생한다고 한다.33,34
Methenamine salts
Methenamine salts 는 소변 내에서 가수분해되어 암모니아와 포름알데히드를 형성한다. 포름알데히드는 광범위한 정균력을 가지며 세균에 의한 내성이 적다. 아직 부작용과 관련한 정보는 부족하나 이러한 효능을 바탕으로 methenamine salts 를 효과적인 재발성 요로감염 예방약제로 개발하려는 노력이 있다. 그러나 이러한 투여를 임상에 적용하기에는 근거가 부족한 상황이다. 다수의 소규모 연구가 이루어지고 있으며 재발성 요로감염의 재발을 억제하는데 있어서 위약군 보다는 좋은 결과를 보였다고 한다.35-39 Cochrane review 에서 methenaminehippurate 성분은 신경인성 방광이나 요로생식기 기형이 없는 환자에서 단기간의 재발성 요로감염 억제에 안전하고 효과가 있을 것으로 보았다.40 (LE: 3)
D-Mannose
Rodent 와 인간 요로상피세포를 이용한 연구에서 D-mannose 를 기반으로 한 FimH(미생물 부착분자) 억제제가 요로상피에 대한 UPEC 의 생착과 침입을 방지함을 확인할 수 있었다.41,42 이 기초과학적 근거를 기반으로 D-mannose 를 인간의 재발성 요로감염 예방에 이용하게 되었으나 임상적인 근거는 아직 없다. 요로계에서 세균 제거를 지연시키는 대식세포의 활동성을 억제할 수 있기에 이론적으로 재발성 요로감염에 효과적일 것이라는 체외 실험적인 근거는 있으나43 type I pili 와 FimH 를 발현하는 특정 균주가 아닌 경우 효과적이지 않다.44
Probiotics
재발성 요로감염 예방을 위해 L. rhamnosus GR-1 과 L. reuteri RC-14 를 포함하는 probiotics를 주 1~2회 질내 투여하는 것은 고려해볼 만하다.45 (LE: 4, GR: C) GR-1 과 RC14 를 포함하는 경구 제품을 매일 복용하는 것 역시 예방법이 될 수 있다.46 (LE: 1, GR: C) 폐경 전 여성에서 Lactobacillus crispatus 를 질내 처치하는 것 또한 재발성 요로감염 예방에 사용될 수 있다.47 (LE: 1, GR: B) 12 개월 간 적어도 1 회 이상의 요로감염 과거력이 있는 100 명의 18 세에서 40 세 사이의 폐경 전 여성을 대상으로 요로감염 완치 후 108CFU/ml 의 L crispatus CTV-05 와 placebo 를 1 일 1 회로 5 일 간 질 내 투여하였고 이후 10 주 간 주 1 회 투여하였다. 10 주 간의 투여 종료 후 L cirspatus CTV-05 를 투여 받은 군에서 위약군에 비해 재발성 요로감염의 빈도가 낮음을 알 수 있었다. (RR 0.5; 95% CI, 0.2-1.2) 질 분비물, 질 소양증 및 복부 불편감과 같은 부작용은 양 군에서 비슷한 빈도였다. (56% for L crispatus CTV-05 and 50% for placebo)
Hyaluronic acid and Chondroitin sulphate
방광 내 glycosaminoglycan (GAG) layer 의 유지를 목표로 Damiano 등 48 은 방광 내 hyaluronic acid 와 chondroitin sulfate (iAluRil®) 투여의 안정성과 효용성을 연구하였다; 잦은 빈도의 재발성 요로감염을 보이는 57 명의 여성을 대상으로 1.6% hyaluronic acid 와 2.0% chondroitin sulfate 50ml 를 투여 받거나 placebo 를 투여 받은 군과 비교하였다. iAluRil® (sodium pentosane sulfate)을 12 개월간 방광내 주입 받은 환자에서 요로감염의 빈도가 의미 있게 감소됨(-86.6% ± 47.6 vs -9.6% ± 24.6%)을 확인할 수 있었다.48 이러한 연구들로 hyaluronic acid 와 chondroitin sulfate 를 이용한 요로감염의 예방이 각광받을 수 있겠으나, 장기간의 연구 결과가 필요하며 범용성, 경제적 효용성 등에 대한 추가적인 연구가 필요하다.
면역강화요법(Immunostimulation)
재발성 요로감염의 예방을 위한 면역증강제의 도입에 다수의 연구가 진행되었다. Naber 등은 면역 강화 예방요법을 위해 요로감염 세균을 죽여 만든 용해물을 이용한 경우를 체계적으로 분석하였다.49 현재 Uro-Vaxom® (OM Pharma, Meyrin, Switzerland)과 SolcoUrovac® (Solco Basel, Basel, Switzerland) 두 개의 제품에 관한 연구가 이루어져 있다. Uro-Vaxom®은 18 가지의 E. coli 균주를 함유한 경구용 캡슐제로 1 일 1 회 복용하며 재발성 단순요로감염의 면역예방요법으로 권고될 수 있다.49,50 (LE: 1, GR: B) 5 개 위약대조군 이중맹검 대조시험을 메타분석한 결과 Uro-Vaxom® 경구 복용으로 요로감염 발생률이 연 0.15-0.82 건으로 요로감염 예방에 위약군보다 효과적이었다.50,51 이후 여성 453 명이 1 년 동안 Uro-Vaxom®을 복용한 대규모 대조시험에서도 요로감염이 34% 감소하였다.51 이 임상시험에서 Uro-Vaxom®은 3 개월 동안 하루 1 회 복용하고 다음 3 개월 동안 중지한 후 그 다음 3 개월 동안 매월 첫 10 일만 하루 1 회 복용하고 다음 3 개월 다시 중지하였다. 국내 연구에 따르면 재발성 방광염이 있는 폐경 전후 여성 42 명이 Uro-Vaxom®을 3 개월 복용한 후 6 개월 추적기간 동안 환자 당 요로감염 발생은 0.35 건으로 치료 전 6 개월간의 4.26 건보다 재발이 훨씬 줄었다. (P<0.001)52 여러 임상시험에서 Uro-Vaxom®은 치명적이거나 중요한 부작용은 없었고 두통이나 소화장애 등의 가벼운 부작용만 관찰되었다.53 유럽비뇨기과학회는 2011 년 지침부터 UroVaxom®을 재발성 요로감염 예방대책의 하나로서 권고하고 있다. 그 외에 SolcoUrovac®은 10 종의 요로병원성의 미생물 균주를 함유한 질정으로서 중등도의 요로감염 예방효과를 보이나 촉진 효과를 위한 복용기간에만 한정된다고 하였다.49,54 최근의 기술적 발전으로 요로감염에 관여하는 E. coli 의 작용에 대해 보다 자세히 알 수 있게 되었으며 이를 통해 보다 오래 지속되고 보다 특이적인 재발성 요로감염 면역증강제 또는 백신이 개발될 수 있을 것이라고 기대된다.
결론
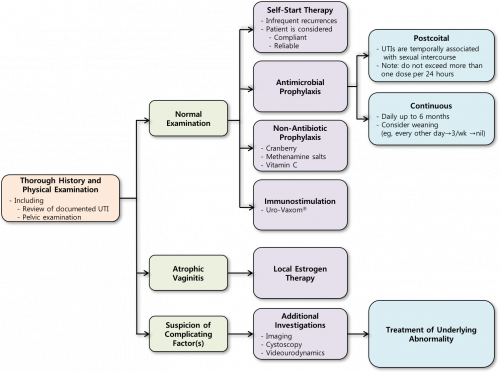
재발성 요로감염은 모든 환자에서 세밀한 병력 청취와 이학적 검사가 필요하고, 이를 통해 동반된 기형이나 교정 가능한 위험인자를 우선 확인토록 해야 한다. 항생제는 가장 효과적인 예방법이긴 하나 부작용이 발생할 수 있다. 항생제의 종류와 형태 및 투여 시기는 환자 개개인의 특성에 따라 적합한 형태로 조절되어야 한다. 항생제 투여 이외의 예방법으로 크랜베리, 비타민 C, methenamine salts 등이 활발히 연구되고 있으나 아직 확실한 증거가 부족하여 Uro-Vaxom®과 같은 면역증강제가 현실적인 대안이 될 수 있겠다. Figure 1 에서 재발성 요로감염의 치료 알고리즘 관련 권장사항을 확인할 수 있다. 재발성 요로감염의 예방과 관련하여 다양하고 새로운 형태의 접근이 이루어져가는 중으로, 추가적인 기초과학 연구와 대규모의 RCT 가 필요하다.
Figure 1. 재발성 요로감염의 치료 알고리즘
참고문헌
1. Fowler JE, Jr., Pulaski ET. Excretory urography, cystography, and cystoscopy in the evaluation of women with urinary-tract infection: a prospective study. N Engl J Med 1981;304:462-5.
2. Foxman B, Gillespie B, Koopman J, Zhang L, Palin K, Tallman P, et al. Risk factors for second urinary tract infection among college women. Am J Epidemiol 2000;151:1194-205.
3. Ikaheimo R, Siitonen A, Heiskanen T, Karkkainen U, Kuosmanen P, Lipponen P, et al. Recurrence of urinary tract infection in a primary care setting: analysis of a 1-year follow-up of 179 women. Clin Infect Dis 1996;22:91-9.
4. Kraft JK, Stamey TA. The natural history of symptomatic recurrent bacteriuria in women. Medicine (Baltimore) 1977;56:55-60.
5. Stamm WE, McKevitt M, Roberts PL, White NJ. Natural history of recurrent urinary tract infections in women. Rev Infect Dis 1991;13:77-84.
6. Mulvey MA, Schilling JD, Hultgren SJ. Establishment of a persistent Escherichia coli reservoir during the acute phase of a bladder infection. Infect Immun 2001;69:4572-9.
7. Rosen DA, Hooton TM, Stamm WE, Humphrey PA, Hultgren SJ. Detection of intracellular bacterial communities in human urinary tract infection. PLoS Med 2007;4:e329.
8. Berry RE, Klumpp DJ, Schaeffer AJ. Urothelial cultures support intracellular bacterial community formation by uropathogenic Escherichia coli. Infect Immun 2009;77:2762-72.
9. van Haarst EP, van Andel G, Heldeweg EA, Schlatmann TJ, van der Horst HJ. Evaluation of the diagnostic workup in young women referred for recurrent lower urinary tract infections. Urology 2001;57:1068-72.
10. Scholes D, Hooton TM, Roberts PL, Stapleton AE, Gupta K, Stamm WE. Risk factors for recurrent urinary tract infection in young women. J Infect Dis 2000;182:1177-82.
11. Foxman B, Chi JW. Health behavior and urinary tract infection in college-aged women. J Clin Epidemiol 1990;43:329-37.
12. Semins MJ, Shore AD, Makary MA, Weiner J, Matlaga BR. The impact of obesity on urinary tract infection risk. Urology 2012;79:266-9.
13. Perrotta C, Aznar M, Mejia R, Albert X, Ng CW. Oestrogens for preventing recurrent urinary tract infection in postmenopausal women. Obstet Gynecol 2008;112:689-90.
14. Brostrom S, Lose G. [Oestrogen for prevention of recurrent urinary tract infections in postmenopausal women--a survey of a Cochrane review]. Ugeskr Laeger 2009;171:2568-71.
15. Raz R, Stamm WE. A controlled trial of intravaginal estriol in postmenopausal women with recurrent urinary tract infections. N Engl J Med 1993;329:753-6.
16. Eriksen B. A randomized, open, parallel-group study on the preventive effect of an estradiol-releasing vaginal ring (Estring) on recurrent urinary tract infections in postmenopausal women. Am J Obstet Gynecol 1999;180:1072-9.
17. Albert X, Huertas I, Pereiro, II, Sanfelix J, Gosalbes V, Perrota C. Antibiotics for preventing recurrent urinary tract infection in non-pregnant women. Cochrane Database Syst Rev 2004:CD001209.
18. Schaeffer AJ, Stuppy BA. Efficacy and safety of self-start therapy in women with recurrent urinary tract infections. J Urol 1999;161:207-11.
19. Wong ES, McKevitt M, Running K, Counts GW, Turck M, Stamm WE. Management of recurrent urinary tract infections with patient-administered single-dose therapy. Ann Intern Med 1985;102:302-7.
20. Gupta K, Hooton TM, Roberts PL, Stamm WE. Patient-initiated treatment of uncomplicated recurrent urinary tract infections in young women. Ann Intern Med 2001;135:9-16.
21. Gupta K, Hooton TM, Naber KG, Wullt B, Colgan R, Miller LG, et al. International clinical practice guidelines for the treatment of acute uncomplicated cystitis and pyelonephritis in women: A 2010 update by the Infectious Diseases Society of America and the European Society for Microbiology and Infectious Diseases. Clin Infect Dis 2011;52:e103-20.
22. Stapleton A, Latham RH, Johnson C, Stamm WE. Postcoital antimicrobial prophylaxis for recurrent urinary tract infection. A randomized, double-blind, placebo-controlled trial. JAMA 1990;264:703-6.
23. Melekos MD, Asbach HW, Gerharz E, Zarakovitis IE, Weingaertner K, Naber KG. Post-intercourse versus daily ciprofloxacin prophylaxis for recurrent urinary tract infections in premenopausal women. J Urol 1997;157:935-9.
24. Guibert J, Humbert G, Meyrier A, Jardin A, Vallancien G, Piccoli S, et al. [Antibioprevention of recurrent cystitis. A randomized double-blind comparative trial of 2 dosages of pefloxacin]. Presse Med 1995;24:213-6.
25. Cetti RJ, Venn S, Woodhouse CR. The risks of long-term nitrofurantoin prophylaxis in patients with recurrent urinary tract infection: a recent medico-legal case. BJU Int 2009;103:567-9.
26. Schmidt DR, Sobota AE. An examination of the anti-adherence activity of cranberry juice on urinary and nonurinary bacterial isolates. Microbios 1988;55:173-81.
27. Lavigne JP, Bourg G, Combescure C, Botto H, Sotto A. In-vitro and in-vivo evidence of dose-dependent decrease of uropathogenic Escherichia coli virulence after consumption of commercial Vaccinium macrocarpon (cranberry) capsules. Clin Microbiol Infect 2008;14:350-5.
28. Howell AB, Botto H, Combescure C, Blanc-Potard AB, Gausa L, Matsumoto T, et al. Dosage effect on uropathogenic Escherichia coli anti-adhesion activity in urine following consumption of cranberry powder standardized for proanthocyanidin content: a multicentric randomized double blind study BMC Infect Dis 2010;10:94.
29. Kontiokari T, Sundqvist K, Nuutinen M, Pokka T, Koskela M, Uhari M. Randomised trial of cranberrylingonberry juice and Lactobacillus GG drink for the prevention of urinary tract infections in women. BMJ 2001;322:1571.
30. Stothers L. A randomized trial to evaluate effectiveness and cost effectiveness of naturopathic cranberry products as prophylaxis against urinary tract infection in women. Can J Urol 2002;9:1558-62.
31. Barbosa-Cesnik C, Brown MB, Buxton M, Zhang L, DeBusscher J, Foxman B. Cranberry juice fails to prevent recurrent urinary tract infection: results from a randomized placebo-controlled trial. Clin Infect Dis 2011;52:23-30.
32. Ochoa-Brust GJ, Fernandez AR, Villanueva-Ruiz GJ, Velasco R, Trujillo-Hernandez B, Vasquez C. Daily intake of 100 mg ascorbic acid as urinary tract infection prophylactic agent during pregnancy. Acta Obstet Gynecol Scand 2007;86:783-7.
33. Carlsson S, Wiklund NP, Engstrand L, Weitzberg E, Lundberg JO. Effects of pH, nitrite, and ascorbic acid on nonenzymatic nitric oxide generation and bacterial growth in urine. Nitric Oxide 2001;5:580-6.
34. Carlsson S, Govoni M, Wiklund NP, Weitzberg E, Lundberg JO. In vitro evaluation of a new treatment for urinary tract infections caused by nitrate-reducing bacteria. Antimicrob Agents Chemother 2003;47:3713-8.
35. Cronberg S, Welin CO, Henriksson L, Hellsten S, Persson KM, Stenberg P. Prevention of recurrent acute cystitis by methenamine hippurate: double blind controlled crossover long term study. Br Med J (Clin Res Ed) 1987;294:1507-8.
36. Gundersen R, Hoivik HO, Osmundsen K. [Frequent cystitis in elderly women. A double-blind comparison of Hiprex and placebo in general practice]. Tidsskr Nor Laegeforen 1986;106:2048-9.
37. Hoivik HO, Gundersen R, Osmundsen K, Halvorsen P, Hjortdahl P, Stokke JG. [Prevention of recurrent cystitis in fertile women. A double-blind comparison of Hiprex and placebo in general practice]. Tidsskr Nor Laegeforen 1984;104:1150-2.
38. Brumfitt W, Cooper J, Hamilton-Miller JM. Prevention of recurrent urinary infections in women: a comparative trial between nitrofurantoin and methenamine hippurate. J Urol 1981;126:71-4.
39. Brumfitt W, Hamilton-Miller JM, Gargan RA, Cooper J, Smith GW. Long-term prophylaxis of urinary infections in women: comparative trial of trimethoprim, methenamine hippurate and topical povidoneiodine. J Urol 1983;130:1110-4.
40. Lee BS, Bhuta T, Simpson JM, Craig JC. Methenamine hippurate for preventing urinary tract infections.Cochrane Database Syst Rev 2012;10:CD003265.
41. Michaels EK, Chmiel JS, Plotkin BJ, Schaeffer AJ. Effect of D-mannose and D-glucose on Escherichia coli bacteriuria in rats. Urol Res 1983;11:97-102.
42. Wellens A, Garofalo C, Nguyen H, Van Gerven N, Slattegard R, Hernalsteens JP, et al. Intervening with urinary tract infections using anti-adhesives based on the crystal structure of the FimH-oligomannose3 complex. PLoS One 2008;3:e2040.
43. Felipe I, Bochio EE, Martins NB, Pacheco C. Inhibition of macrophage phagocytosis of Escherichia coli by mannose and mannan. Braz J Med Biol Res 1991;24:919-24.
44. van der Bosch JF, Verboom-Sohmer U, Postma P, de Graaff J, MacLaren DM. Mannose-sensitive and mannose-resistant adherence to human uroepithelial cells and urinary virulence of Escherichia coli. Infect Immun 1980;29:226-33.
45. Anukam KC, Osazuwa E, Osemene GI, Ehigiagbe F, Bruce AW, Reid G. Clinical study comparing probiotic Lactobacillus GR-1 and RC-14 with metronidazole vaginal gel to treat symptomatic bacterial vaginosis. Microbes Infect 2006;8:2772-6.
46. Wagenlehner FM, Vahlensieck W, Bauer HW, Weidner W, Piechota HJ, Naber KG. Prevention of recurrent urinary tract infections. Minerva Urol Nefrol 2013;65:9-20.
47. Stapleton AE, Au-Yeung M, Hooton TM, Fredricks DN, Roberts PL, Czaja CA, et al. Randomized, placebo-controlled phase 2 trial of a Lactobacillus crispatus probiotic given intravaginally for prevention of recurrent urinary tract infection. Clin Infect Dis 2011;52:1212-7.
48. Damiano R, Quarto G, Bava I, Ucciero G, De Domenico R, Palumbo MI, et al. Prevention of recurrent urinary tract infections by intravesical administration of hyaluronic acid and chondroitin sulphate: a placebo-controlled randomised trial. Eur Urol 2011;59:645-51.
49. Naber KG, Cho YH, Matsumoto T, Schaeffer AJ. Immunoactive prophylaxis of recurrent urinary tract infections: a meta-analysis. Int J Antimicrob Agents 2009;33:111-9.
50. Bauer HW, Rahlfs VW, Lauener PA, Blessmann GS. Prevention of recurrent urinary tract infections with immuno-active E. coli fractions: a meta-analysis of five placebo-controlled double-blind studies. Int J Antimicrob Agents 2002;19:451-6.
51. Bauer HW, Alloussi S, Egger G, Blumlein HM, Cozma G, Schulman CC, et al. A long-term, multicenter, double-blind study of an Escherichia coli extract (OM-89) in female patients with recurrent urinary tract infections. Eur Urol 2005;47:542-8; discussion 8.
52. Kim KS, Kim JY, Jeong IG, Paick JS, Son H, Lim DJ, et al. A prospective multi-center trial of Escherichia coli extract for the prophylactic treatment of patients with chronically recurrent cystitis. J Korean Med Sci 2010;25:435-9.
53. Ha US, Cho YH. Immunostimulation with Escherichia coli extract: prevention of recurrent urinary tract infections. Int J Antimicrob Agents 2008;31 Suppl 1:S63-7.
54. Uehling DT, Hopkins WJ, Elkahwaji JE, Schmidt DM, Leverson GE. Phase 2 clinical trial of a vaginal mucosal vaccine for urinary tract infections. J Urol 2003;170:867-9.